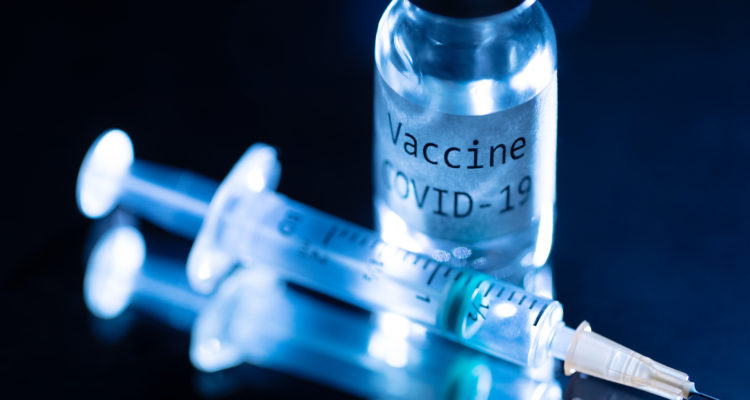
El anuncio de una efectividad superior al 90% de dos vacunas, prácticamente en la misma semana, ha devuelto el optimismo en la lucha contra la covid-19.
Sin embargo, diversos especialistas como Mariangela Simao, directora adjunta en la OMS y responsable del área acceso a medicamentos y vacunas, advierten que es demasiado pronto para cantar victoria. Quedan muchos problemas por resolver, incluidas etapas de validación, autorizaciones para su puesta en el mercado, distribución y accesibilidad.
La multiplicación de anuncios sobre vacunas candidatas para combatir la covid-19, no debe hacer perder de vista el contexto general de las vacuna, como lo recuerda Kate O’Brien, experta en inmunología de la OMS: “Tenemos una gran cantidad de vacunas que están disponibles, como la del sarampión que tiene más del 95% de eficacia, y aun así todavía tenemos brotes de esta enfermedad”.
La directora adjunta de la OMS señala que la distribución será complicada y limitada, al menos hasta mediados de 2021. Teniendo en cuenta que algunos países ya han hecho contratos unilaterales, reduciendo así el número de dosis para el resto. La producción, al menos en una primera etapa, no será ilimitada.
Moderna, por ejemplo, ya ha advertido que de aquí a finales de año próximo solo podrá ofrecer dosis a menos del 7% de la población mundial, especialmente en los países ricos.
En este sentido circulan llamados de ONG a compartir la propiedad intelectual y la tecnología para producir vacunas en forma masiva, mientras organizaciones no gubernamentales como Oxfam critican a la Unión Europea que a finales de agosto anunció un pedido de 80 millones de dosis de la futura vacuna de Moderna, sin especificar claramente los criterios de accesibilidad.
Pfizer y Moderna, cabeza a cabeza
Los laboratorios Pfizer y Moderna, a la cabeza en la carrera por la vacuna contra la Covid-19 afirman estar en condiciones de entregar las primeras dosis antes de finales de año, pero numerosos especialistas piensan que solo podrán hacerlo a comienzos del año próximo, ya que los ensayos siguen aún en curso.
En el caso de Moderna, 150 voluntarios deben contraer la enfermedad, para tener suficientes observaciones, y por el momento sólo disponen de 95. Sin olvidar la luz verde de las autoridades sanitarias, en el caso de estados unidos la “Food and Drug Administration” (FDA), en Europa la agencia europea de medicamentos EMA, que actualmente estudia los primeros datos clínicos de 7 laboratorios, entre los cuales Pfizer, Astrazeneca y Moderna.
Si es verdad que existe cooperación, también hay competencia entre las diferentes compañías farmacéuticas que se hallan en plena carrera por ser los primeros en conseguir la vacuna, por lo cual los anuncios -que repercuten directamente en la bolsa- hay que estudiarlos en detalle.
Según sus proyecciones, los laboratorios han previsto entregar unas cincuenta millones de vacunas este año, aunque probablemente estas cifras sólo serán una realidad concreta el año próximo, cuando efectivamente podrán hacer frente a la demanda con más de mil millones de dosis disponibles.
Pero tal vez, incluso en ese momento, los indígenas del Chaco no tendrán las mismas facilidades que un europeo para a acceder a la vacuna.







 Enviando corrección, espere un momento...
Enviando corrección, espere un momento...