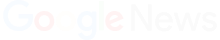La resistencia en infecciones de la sangre –que pueden llevar a una sepsis– causó unos 370.000 fallecimientos e incidió en otros 1,5 millones.
Las infecciones por superbacterias mataron a 1,2 millones de personas en 2019, según un estudio publicado este jueves por The Lancet, que los autores describieron como la evaluación más completa del impacto de la resistencia a los antimicrobianos hasta la fecha.
La Investigación global sobre la resistencia antimicrobiana (GRAM, en inglés) calcula que otros 4,95 millones de muertes ese año pueden asociarse con esas infecciones, aunque no fueran su causa directa.
Los autores advierten de que la resistencia a los antibióticos de bacterias causantes de infecciones como la neumonía u otras de la sangre o intraabdominales (derivadas por ejemplo de la apendicitis) provoca ahora más fallecimientos anuales que el sida y la malaria, con 860.000 y 640.000 registrados por estas enfermedades en 2019, respectivamente.
Este estudio es el mayor de este tipo realizado hasta el momento y los investigadores analizaron las muertes vinculadas a 23 patógenos y 88 combinaciones de medicamentos para patógenos en un total de 204 países y territorios.
La resistencia antimicrobiana (AMR)
Los expertos, de las universidades de Washington (Estados Unidos) y Oxford (Inglaterra), usaron un modelo estadístico para calcular el impacto global de la resistencia antimicrobiana (AMR, en inglés), en base a 471 millones de historiales individuales obtenidos de varias fuentes.
Su análisis demuestra que la AMR en infecciones del sistema respiratorio inferior, como la neumonía, causó más de 400.000 muertes de forma directa y se asoció con otros 1,5 millones.
Por su parte, la resistencia en infecciones de la sangre –que pueden llevar a una sepsis– causó unos 370.000 fallecimientos e incidió en otros 1,5 millones, mientras que la resistencia antimicrobiana mostrada por infecciones intraabdominales provocó unos 210.000 decesos en 2019 y estuvo vinculada a otros 800.000.
Niños pequeños, el grupo con más riesgo
Aunque la AMR afecta a todas las edades, el grupo con más riesgo son los niños pequeños, con una de cada cinco muertes atribuida al fenómeno ocurrida entre niños de menos de 5 años.
Las zonas con más fallecimientos motivados por la resistencia a los antibióticos fueron el África subsahariana y el sur de Asia, con 24 y 22 por cada 100.000 habitantes, respectivamente. En cuanto a las muertes asociadas, se estima que fueron en esas regiones de 99 y 77 por 100.000 personas.
En los países de ingresos altos, la AMR fue la causa directa de 13 muertes por cada 100.000 habitantes en 2019 e incidió de alguna manera en 56 decesos por cada 100.000 personas.
De los 23 patógenos estudiados, la resistencia de solo seis de ellos (E. coli; S. aureus; K. pneumoniae; S. pneumoniae; A. baumannii y P. aeruginosa) llevó a 929.000 muertes y estuvo vinculada a otras 3,57 millones.
Una de las combinaciones patógeno-medicamento –el estafilococo aureus (causante de infecciones de la piel) resistente a la meticilina– causó directamente 100.000 muertes en el año estudiado.
Resistencia a las fluoroquinolonas y los betalactámicos
La resistencia a dos clases de antibióticos habitualmente administrados contra infecciones graves -las fluoroquinolonas y los betalactámicos- supone aproximadamente un 70 % de las muertes causadas por AMR, dice el estudio.
El impacto de los patógenos varía según el lugar, y mientras en el África subsahariana buena parte de las muertes vinculadas a la resistencia antimicrobiana son por S. pneumonia, en los países ricos se deben sobre todo a S. aureus y E. coli.
Los autores, que reconocen que hay que seguir estudiando el fenómeno con datos más precisos de ciertos países donde escasean, recomiendan tomar medidas cuanto antes para limitar el desarrollo de resistencia a los antibióticos.
Entre otras cosas, aconsejan a los Gobiernos y autoridades sanitarias “optimizar el uso de los antibióticos existentes” y no recetarlos sin motivo; controlar y hacer un mejor seguimiento de las infecciones y proporcionar más fondos para desarrollar nuevos antibióticos y tratamientos.
Crisis sanitaria mundial
La resistencia a los antimicrobianos se produce cuando las bacterias evolucionan para ser inmunes a los antibióticos.

La Organización Mundial de la Salud la ha declarado una crisis sanitaria mundial y ha creado un grupo de trabajo para estudiar tratamientos alternativos.
Uno de los campos de investigación es el de los virus devoradores de bacterias, llamados bacteriófagos o simplemente fagos.
Un estudio de caso publicado el martes en Nature Communications describe cómo los médicos belgas utilizaron esta terapia para curar a un paciente cuya pierna estaba infectada desde hacía casi dos años.
Anais Eskenazi, coautora del estudio y encargada del cuidado del paciente, describió cómo un laboratorio de Georgia encontró el virus en una muestra de agua del alcantarillado, donde abundan los fagos debido a las masas de bacterias.
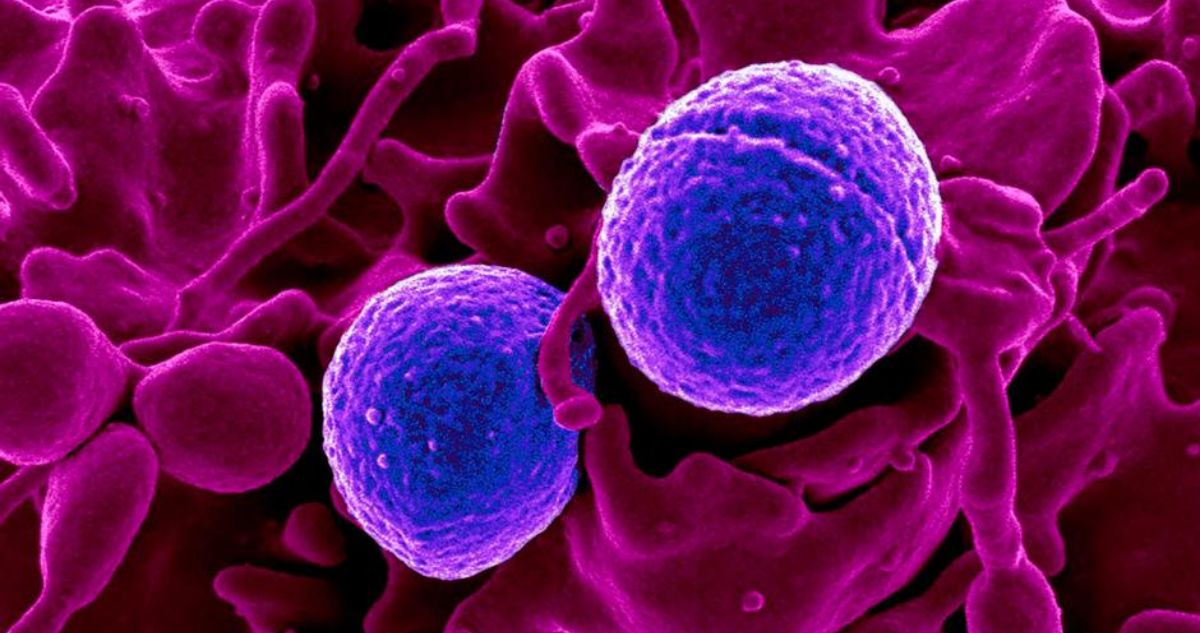
Aislaron el que determinaron que podría atacar a la superbacteria específica del paciente, la Klebsiella pneumoniae, resistente a los antibióticos. El tratamiento podría aplicarse por vía intravenosa, oral o tópica -en el exterior del cuerpo-, explicó Eskenazi a la AFP.
“En este caso, utilizamos la administración tópica… la herida se enjuagó con una solución que contenía fagos”, dijo. Combinada con antibióticos, la terapia con fagos curó la infección en tres meses, según el estudio.
Mientras que los fagos se han utilizado para tratar infecciones en Rusia y Europa del Este durante más de un siglo, en la UE (Unión Europea) y Estados Unidos se pasan por alto.
Eskenazi señaló que entre las posibles razones para ello se encuentra el miedo a la exposición a los virus, aunque los fagos no suponen una amenaza para las personas. “Los bacteriófagos no pueden infectar las células humanas, son específicos de las bacterias”, aclaró







 Enviando corrección, espere un momento...
Enviando corrección, espere un momento...